La FDA propose d'alléger les tests pour accélérer le développement des biosimilaires
information fournie par Zonebourse 09/03/2026 à 20:43
L'agence propose notamment de réduire certaines études pharmacocinétiques lorsque les données scientifiques existantes sont jugées suffisantes. Selon la FDA, cette mesure pourrait diminuer jusqu'à 50% le coût de ces essais, soit environ 20millions de dollars pour les développeurs. L'objectif est de faciliter l'arrivée de versions moins coûteuses des médicaments biologiques, dont 82 biosimilaires ont déjà été approuvés aux États-Unis.
Le projet prévoit aussi de permettre aux entreprises de s'appuyer, dans certains cas, sur des données cliniques provenant de versions comparables du médicament de référence approuvées hors des États-Unis. Parallèlement, la FDA a retiré une directive publiée en 2015 sur la démonstration de l'équivalence des biosimilaires, estimant qu'elle ne reflète plus son approche actuelle après plusieurs années d'expérience dans l'évaluation de ces produits
A lire aussi
-
![Monica Franco, mère de Bryan Ledesma, un homme tué dans une opération militaire en Equateur, touche la tombe de son fils à Milagro, dans la province de Guayas, le 23 mai 2026 ( AFP / Marcos PIN )]()
Monica Franco est inconsolable. Depuis trois mois, elle pleure son fils Bryan, "battu à mort" lors d'une opération militaire antidrogue dans le sud-ouest de l'Equateur. Ce jeune homme de 28 ans est l'une des victimes présumées des dérives de l'armée dans la lutte ... Lire la suite
-
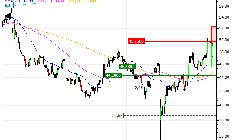
![Sodexo : Correction technique anticipée (A47TS)]()
(Zonebourse.com) La reprise technique dernièrement observée sur Sodexo devrait trouver un point d'arrêt dans la zone de cours actuelle. Le timing apparaît pertinent pour anticiper des prises de bénéfices, avec les 45.6 EUR comme principal objectif, zone de convergence ... Lire la suite
-
![( AFP / JEAN-FRANCOIS MONIER )]()
Le géant pharmaceutique britannique GSK a annoncé mardi un accord pour acquérir la société biopharmaceutique américaine Nuvalent, spécialisée dans le développement de thérapies contre le cancer, "pour un montant de 10,6 milliards de dollars" (9,18 milliards d'euros). ... Lire la suite
-
![Un secouriste porte un chien de sauvetage lors d'opérations de recherche au niveau d'un bâtiment effondré, le 9 juin 2026 à General Santos aux Philippines ( AFP / Jam STA ROSA )]()
Des blessés soignés dehors en pleine chaleur, des secours ralentis par les répliques et des accès coupés : au lendemain du puissant séisme qui a frappé le sud des Philippines faisant au moins 41 morts, des milliers de personnes sont toujours déplacées mardi. Le ... Lire la suite
Mes listes
Une erreur est survenue pendant le chargement de la liste
valeur |
dernier |
var. |
|---|---|---|
| 92,72 | -1,48% | |
| 8 262,68 | +0,77% | |
| 52,95 | -2,67% | |
| 0,274 | +2,62% | |
| 156,2 | -0,16% |



0 commentaire
Vous devez être membre pour ajouter un commentaire.
Vous êtes déjà membre ? Connectez-vous
Pas encore membre ? Devenez membre gratuitement
Signaler le commentaire
Fermer