
Le développement d'Elafibranor dans la stéatohépatite non-alcoolique (NASH) reste bien sûr le point focal des investisseurs. (crédit : Genfit)
La biotech lilloise a publié, jeudi 6 décembre les données cliniques de phase II, obtenues avec Elafibranor, son produit phare, dans la cholangite biliaire primitive (PBC), chez 45 patients. Ces résultats sont sans nuage. Le produit phare de la biotech lilloise, qui appartient à la classe des inhibiteurs des PPAR alpha et delta, a permis une réduction de 48% de l'alkaline phosphatase (ALP) chez les patients, à la dose 80 mg (et de -41% à la dose 120 mg) en 12 semaines de traitement, contre une hausse de 3% dans le bras placebo. Cette différence sur l'ALP, le critère principal de l'essai, est statistiquement significative.
Sur le plan de l'efficacité, Elafibranor fait mieux qu'OCA, le seul produit aujourd'hui approuvé pour le traitement de cette maladie du foie (il avait affiché en phase III des taux de réductions situés entre -33 et -39 % d'ALP). Il est au coude-à-coude avec le Seladelpar, développé par l'américain Cymabay ( -21 à -45% d'ALP selon les doses) et semble distancer GKT831 de Genkyotex (-17% mais en seulement six semaines). D'autres marqueurs sont signalés comme positifs, sans être toutefois détaillés, tandis qu'une « amélioration du prurit est observée ». Au terme d'une phase III qui reste à mener, Elafibranor peut espérer détrôner un roi, OCA, très contesté. Ce produit commercialisé par la biotech américaine Intercept, provoque une hausse du prurit et d'autres effets secondaires.
Partenariat dans le test sanguin ?
Le développement d'Elafibranor dans la stéatohépatite non-alcoolique (NASH) reste bien sûr le point focal des investisseurs. Si NASH et PBC sont deux pathologies bien différentes, le mécanisme d'action sur le métabolisme et la dimension inflammatoire sont parallèles. Ces résultats confortent donc les chances d'Elafibranor de se différencier sur le front de l'efficacité et de la tolérance face à OCA, lui aussi développé dans la NASH, ainsi qu'aux autres actifs actuellement en phase III dans cette indication (voir tableau ci-dessous).
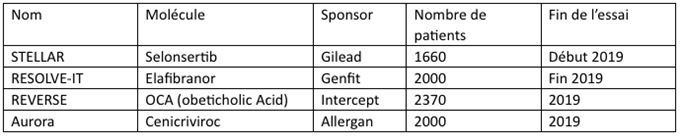
Les différents candidats médicaments en phase III dans la NASH. (crédit : Biotech Finances)
La biotech a également annoncé, ces derniers jours, le lancement prochain d'un essai de phase II avec nitazoxanide (NTX) chez des patients souffrant de NASH et ayant une fibrose de stade 2 ou 3 (sur une échelle allant de 0 à 4). Cette molécule prescrite comme antiparasitaire a été repositionnée (et re-brevetée) par Genfit dans les maladies fibrosantes du foie. Elle va permettre à la société de renforcer un peu son pipeline, avec un produit dont le mécanisme d'action, centré sur la fibrose, est présenté comme complémentaire avec celui d'Elafibranor, surtout actif sur le «versant» métabolique de la maladie.
Enfin, dans les semaines à venir, la société devrait dévoiler un partenariat industriel pour le développement d'un test sanguin de diagnostic de la NASH, alternatif à la biopsie aujourd'hui pratiquée en essais cliniques pour évaluer l'avancée de la maladie. Objectif affiché des dirigeants : mettre un test viable à disposition des centres d'investigation dès l'an prochain et assurer un lancement commercial d'ici début 2021, c'est-à-dire en même temps qu'Elafibranor.
Autant d'arguments pour bétonner le dossier Genfit, dont les dirigeants s'efforcent actuellement de vanter les mérites auprès des investisseurs américains, en vue d'une toute prochaine IPO sur le Nasdaq.
Biotech Finances - «Biotech Finances est un média spécialisé sur l'écosystème francophone des biotechs et des medtechs»



1 commentaire
Vous devez être membre pour ajouter un commentaire.
Vous êtes déjà membre ? Connectez-vous
Pas encore membre ? Devenez membre gratuitement
Signaler le commentaire
Fermer