FEU VERT AUX USA A LA COMMERCIALISATION DU "VIAGRA FÉMININ"
par Toni Clarke et Ransdell Pierson
WASHINGTON (Reuters) - Les autorités sanitaires américaines ont approuvé mardi, après l'avoir refusée à deux reprises, la commercialisation d'un traitement contre les troubles du désir sexuel chez la femme, avec un avertissement sur les effets potentiellement dangereux de ce médicament.
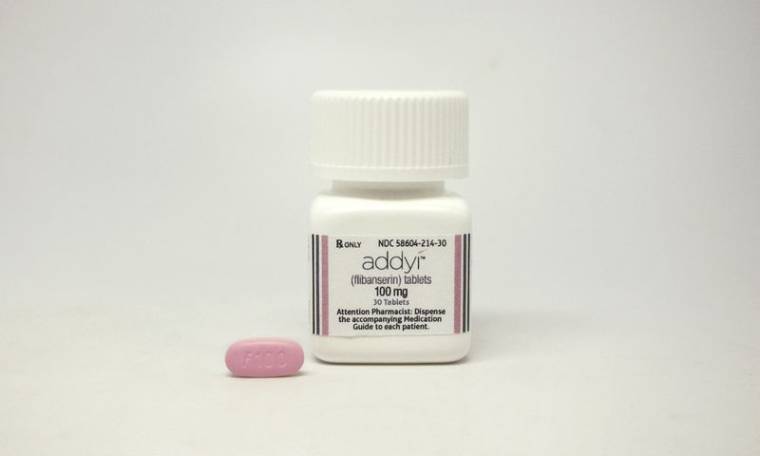
La Food and Drug Administration (FDA) souligne en outre que ce traitement, la flibansérine, qui sera commercialisée sous la marque Addyi par le laboratoire Sprout Pharmaceuticals, ne pourra être délivré que sur ordonnance.
Des médias ont baptisé cette pilule rose le "Viagra féminin" même s'il n'agit pas de la même manière que les pilules bleues vendues depuis 1998 par Pfizer pour traiter les troubles de l'érection chez l'homme.
Initialement développée par le laboratoire allemand Boehringer-Ingelheim dans le cadre de recherches sur le traitement de la dépression, la flibansérine agit sur la stimulation sexuelle dans le cerveau alors que le Viagra favorise l'afflux de sang vers les parties génitales. Ce traitement qui doit être pris quotidiennement appartient ainsi à la classe des inhibiteurs sélectifs de la recapture de la sérotonine (ISRS, ou SSRI en anglais), qui comprend les antidépresseurs comme le Prozac.
La FDA a refusé en 2010 une première demande d'autorisation de mise sur le marché, un comité consultatif ayant conclu que les bénéfices du traitement étaient inférieurs aux risques associés à sa prise.
Boehringer-Ingelheim a ensuite cédé la flibansérine au laboratoire Sprout, qui n'est pas coté en Bourse. Ce dernier a effectué de nouveaux tests et soumis une nouvelle demande à la FDA, qui a encore émis un refus en 2013.
Cette décision a conduit Sprout à mener campagne contre la FDA, avec l'appui d'associations féministes, en accusant les autorités sanitaires américaines de sexisme puisqu'elles avaient approuvé le Viagra. Les membres de la FDA ont vigoureusement rejeté ces accusations.
RISQUES DE SYNCOPE
La flibansérine est destinée aux femmes non ménopausées pour lesquelles le trouble du désir sexuel entraîne une souffrance psychologique.
"Il s'agit de la plus importante avancée pour la santé sexuelle de la femme depuis l'avènement de la pilule contraceptive", s'est réjouie la Ligue nationale des consommateurs (National Consumers League) dans un communiqué. "Cela valide (et) légitime la sexualité féminine en tant qu'aspect important de la santé."
Les détracteurs de ce médicament jugent en revanche que le gain de libido montré par les essais cliniques est trop faible par rapport aux risques encourus, comme une baisse de la pression artérielle, voire une syncope, notamment en cas de consommation d'alcool durant la prise du traitement.
L'association de consommateurs Public Citizen prédit ainsi que l'Addyi sera retiré du marché dans les prochaines années en raison des "graves dangers pour la femme, avec de faibles avantages". "Malheureusement, nous n'avons pas fini d'entendre parler de ce médicament", assure cette association.
L'annonce du feu vert de la FDA à la commercialisation de la flibansérine a fait bondir d'environ 30% l'action de Palatin Technologies dans les transactions après la clôture à la Bourse de New York.
Ce laboratoire est en train de développer un traitement concurrent, la brémélanotide, dont les essais cliniques sont entrés dans leur dernière phase. Selon Palatin Technologies, ce traitement fonctionne différemment de l'Addyi en cherchant à activer certaines connexions cérébrales et il ne se prend qu'en cas de besoin, et non tous les jours.
(Bertrand Boucey pour le service français)


0 commentaire
Vous devez être membre pour ajouter un commentaire.
Vous êtes déjà membre ? Connectez-vous
Pas encore membre ? Devenez membre gratuitement
Signaler le commentaire
Fermer